Les lampes à décharge

Historique
Plusieurs lampes à décharges expérimentales sont mises au point en laboratoire durant la seconde partie du 19ème siècle. C'est finalement le britannique Cooper-Hewitt qui présente en 1901 la première lampe à décharge réellement exploitable. Celle-ci se présente sous la forme d’un tube hermétique dans lequel est inséré un mélange gazeux, terminé par deux électrodes. Depuis cette époque, l'utilisation des lampes à décharge n'a cessé de croitre. Au point d'être quasiment les seules à être utilisées pour l'éclairage public durant la seconde moitié du 20ème siècle.
Deux propriétés physiques fondamentales
Décharge et arc électrique
On appelle « décharge électrique » l'ensemble des phénomènes qui résultent du passage d'un courant électrique d'un conducteur solide à un milieu gazeux conducteur. Le phénomène physique qui en est à l’origine est décrit dans la section « Lumière » de ce site web. On peut résumer la décharge à ceci : « le fait de faire passer un courant électrique dans un milieu gazeux produit de la lumière par la création d’un arc électrique ». Ce phénomène est notamment observable à l’occasion d’un ou de plusieurs éclairs pendant un orage.
Le principe général d'une lampe à décharge consiste à appliquer une différence de potentiel électrique (une tension électrique) entre deux électrodes, séparées par un milieu rempli de gaz. L'application de cette différence de potentiel provoque une ionisation du milieu gazeux, puis un courant électrique allant d'une électrode à l'autre. Les ions et les électrons se déplacent vers l’une ou l’autre électrode en fonction de leur polarité. Ces déplacements provoquent des « collisions » entre les électrons et les ions. Celles-ci excitent les ions ou molécules de gaz. Ceux-ci contiennent un surplus d'énergie qui les rend instable et réémettent cette énergie sous forme de « rayonnement électromagnétique ». Une partie de celui-ci est visible par l’œil humain, on le qualifie alors de « lumière ».
Phénomène du rayonnement électromagnétique
1 - Circulation des électrons à l'application d'une tension.

2 - Les électrons acquierent de l'énergie lorsqu'ils sont en circulation.
3 - Les électrons heurtent les atomes de gaz durant leur déplacement.


4 - Les électrons cèdent l'énergie qu'ils ont accumulé aux atomes de gaz durant la collision.
5 - Les atomes de gaz accumulent un excès d'énergie qu'ils libèrent sous forme de rayonnement.


Décharge et couleur de la lumière émise
Un second phénomène physique est à l’origine de la couleur de la lumière émise dans un milieu gazeux. Il est également décrit dans la section « Lumière » de ce site web. Les matériaux sont tous dotés de propriétés intrinsèques qui impliquent qu’ils rayonnent à certaines longueurs d’ondes (« couleurs ») définies lorsque leurs atomes se désexcitent. Autrement dit, la nature du gaz dans lequel circule un courant électrique joue sur la couleur de la lumière générée. En fonction du mélange gazeux qui est introduit dans la lampe, celle-ci rayonne dans certaines gammes de couleurs. Celles-ci varient en fonction de la température.
Grâce à cette propriété, il devient possible d’émettre une lumière d'une certaine couleur en insérant un mélange gazeux dans le milieu on l'on crée la décharge. Ci-dessous un extrait du site Wikipédia qui illustre quelques applications possibles :
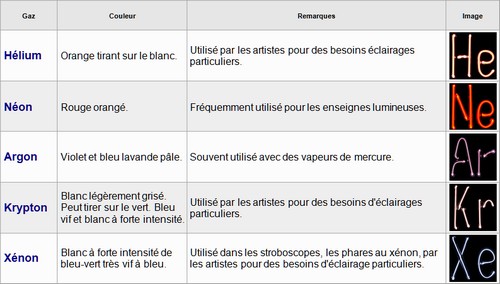
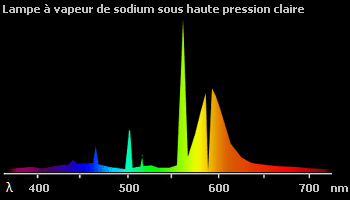
Il est également important de préciser que pour beaucoup de milieux gazeux, le rayonnement provoqué par une décharge contient de nombreux rayons non-visibles (ultraviolets ou infrarouges). Aussi, indépendamment de la couleur émise, il existe des mélanges gazeux qui sont plus efficaces que d'autres d'un point de vue rapport lumière émise sur énergie totale rayonnée. On parle « d'efficacité lumineuse ». La vapeur de sodium est le milieu gazeux le plus efficace qui ait été découvert.
Décharge dans la vapeur de mercure
Décharge dans la vapeur de sodium


Constitution de la lampe à décharge
Depuis la lampe de Cooper-Hewitt en 1901, les lampes à décharge se sont très nettement diversifiées, notamment en fonction du mélange de gaz utilisé jouant sur la couleur de la lumière émise. Les lampes à décharge ont toutefois en commun d’être constituées, d’une manière générale :
Lampes à décharge luminescente sous basse pression
Les « tubes fluorescents » et les lampes « LPS » (Low Pressure Sodium) sont les deux grandes familles de lampes renfermant un gaz sous basse pression. Les premières produisent de la lumière blanche, avec de la vapeur de mercure et une matière fluorescente. Les secondes produisent une lumière jaune-œuf avec de la vapeur de sodium. Dans tous les cas, ces lampes sont constituées :
Schéma d'un tube fluorescent

Lampe à vapeur de sodium sous basse pression PHILIPS SOX

Lampes à décharge luminescente sous haute pression
Les « ballons fluorescents » et les lampes « HPS » (High Pressure Sodium) ont longtemps été les deux principales familles de lampes renfermant un gaz sous basse pression. A partir de la fin des années 1990, les lampes « MH » (Metal Halide) se sont généralisées. Les ballons fluorescents produisent de la lumière blanche à reflets violacés, avec de la vapeur de mercure et une matière fluorescente. Les lampes HPS produisent une lumière blanche à reflets orangés, avec de la vapeur de sodium. Les lampes MH produisent une lumière blanche chaude ou froide, en fonction du mélange gazeux introduit (il en existe plusieurs qui sont commercialisés). Dans tous les cas, ces lampes sont constituées :
Nota : En 1994, PHILIPS présente des lampes MH de nouvelle génération (baptisées « MASTERColour »), équipées d'un brûleur céramique qui remplace le tube à décharge.
Photo d'une lampe à décharge à vapeur de sodium haute pression (HPS).

Schéma d'un tube à décharge

Dans une lampe pour gaz sous haute pression, le tube à décharge (en quartz, en alumine ou en céramique) a une température de fusion très élevée. Il n'est pas affecté par la chaleur extrême produite par l’arc électrique dans la vapeur gazeuse sous haute pression. La zone autour du tube à décharge, à l'intérieur de l'enveloppe en verre, contient un gaz inerte (azote) afin d'empêcher l'oxydation des pièces internes. L'enveloppe de verre a egalement pour but de protéger le milieu extérieur de tout contact avec les éléments conducteurs.
Lampes HID (High-Intensity Discharge)

De gauche à droite, de haut en bas :
Ballon fluorescent (PHILIPS HPL-N - 80W) : Lampe à vapeur de mercure sous haute pression avec poudre fluorescente.
Ballon diffusant (LUCALOX LU250 - 250W) : Lampe à vapeur de sodium sous haute pression avec poudre diffusante.
Lampe HPS claire (OSRAM SON-T - 150W) : Lampe à vapeur de sodium sous haute pression translucide.
Lampe MH claire (PHILIPS Master HTI-P Plus - 400W) : Lampe aux halogénures métalliques sous haute pression translucide.
Lampe LPS (Marque inconnue)
Fonnctionnement de la lampe à décharge
Régime transitoire et régime établi
Une des raisons qui explique pourquoi les lampes à décharge sont quasi exclusivement réservé au milieu professionnel est qu’elles nécessitent un appareillage dédié pour fonctionner. Contrairement aux lampes à incandescence qui peuvent être directement branchées sur le secteur, les lampes à décharge ne peuvent généralement fonctionner sans être accompagnées d'au moins un des éléments suivants :

À température ambiante, les éléments métalliques qui assurent le passage du courant électrique dans le tube à décharge ne sont pas à l’état gazeux (état liquide pour le mercure, état solide pour le sodium). Les deux électrodes sont ainsi séparées par un milieu « isolant » qui s’apparente à du vide (gaz neutre). La tension de 230 Volts / 50 Hz du secteur est généralement trop faible pour permettre le passage du courant électrique dans un tel milieu. Les composants cités ci-dessus permettent de fournir, sur une courte durée, une tension très élevée (généralement plusieurs milliers de Volts) pour forcer le passage du courant électrique au démarrage. Par la suite, celui-ci chauffe l’intérieur du tube, ce qui vaporise les éléments métalliques à l’intérieur du tube (mercure, sodium ou autres éléments métalliques). Lorsque la lampe est en régime établi, la vapeur de mercure ou de sodium rend le milieu « conducteur », permettant un passage du courant électrique sous 230 Volts. Le ballast joue alors un rôle de régulateur de courant au sein de la lampe, pour protéger cette dernière (il se comporte comme une bobine accompagnée d'une résistance en série). Vous trouverez plus d’information concernant ces composants dans la section « Appareillage » de ce site.
La nécessité d’utiliser un tel appareillage, souvent encombrant et lourd (parfois plusieurs kilogrammes), rend la plupart des lampes à décharge inadaptées à l’usage domestique, où l’habitant préfère installer une simple lampe à incandescence qui se suffit à elle-même. Ce n’est qu’au milieu des années 2000, avec la généralisation des lampes fluocompactes (tubes fluorescents miniaturisés contenant leur appareillage intégré), que la question du remplacement des lampes à incandescence par des lampes à décharge dans les habitations se pose. Ceci avant la généralisation des LED quelques années plus tard.
Gaz de travail et gaz d’emprisonnement
Les appellations courantes des lampes à décharge les plus utilisées, lampes « à vapeur de mercure », ou « à vapeur de sodium » laisse penser que les seuls éléments cités dans l’appellation, c'est-à-dire le mercure et le sodium dans les deux exemples respectifs cités, sont présents dans le tube à décharge. Le mélange gazeux introduit est généralement bien plus complexe.
Pour qu’une décharge produise un rayonnement souhaité, il est nécessaire d’utiliser un gaz favorisant un rayonnement visible. Celui-ci est principalement assuré par le mercure ou le sodium dans les lampes « à vapeur de mercure » et « à vapeur de sodium ». Les éléments responsables de l’émission de lumière sont généralement appelés « éléments principaux ». Introduire les seuls éléments principaux est toutefois insuffisant dans la majorité des cas. De nombreux facteurs s’opposent en effet à ce que ce rayonnement se produise de façon optimale.
Premièrement, les éléments principaux ont un rendement optimal à un niveau de pression défini, laquelle est liée à la température. En effet, à très faibles niveau de pression, plus la pression augmente, plus les interactions sont nombreuses et plus le rayonnement émis est intense. Toutefois, au-delà d’un niveau de pression optimal, les effets d’auto-absorption augmentent (absorption des photons émis par les atomes ou ions de l’élément principal), et la partie du rayonnement qui s’échappe diminue. C’est à de très faibles valeurs de pression que les éléments principaux (tels que le mercure et le sodium) ont un rendement lumineux optimal (environ 1 Pascal pour le mercure)..
Deuxièmement, les particules chargées ont une tendance naturelle à se diffuser vers les zones les plus froides du tube à décharge, c'est-à-dire les parois. Or, c’est lorsque la distribution thermique est la plus équilibrée que le rendement lumineux est optimal..
Afin de pallier à ces difficultés causées par la nécessité d’avoir une faible pression de l’élément principal et une distribution thermique la plus équilibrée possible au sein du tube à décharge, un ensemble gazeux est introduit dans le tube où sont mélangés :
Gaz de travail
Le gaz de travail utilisé doit être constitué d’éléments qui respectent certaines conditions. Les plus importantes sont celles-ci :
Ces caractéristiques sont intrinsèques à chaque élément chimique. Les métaux, et notamment les alcalins (dont fait partie le sodium) et les terres rares sont ceux qui respectent le mieux la première condition. Ils doivent également pouvoir être facilement vaporisés, être peu susceptibles de réagir chimiquement avec les constituants du tube, ou encore être bon marché. Le mercure et le sodium ont été les deux éléments les plus rapidement adoptés. Dans les lampes à décharge d’aujourd’hui, le « gaz de travail » est généralement un amalgame de plusieurs éléments :

Gaz d’emprisonnement
La densité du gaz d’emprisonnement doit être suffisamment importante pour contribuer aux interactions des éléments principaux. Sa pression est bien supérieure à celle du gaz de travail. Malgré cela, il ne doit pas altérer le rayonnement émis par les éléments principaux. Ainsi, à l’inverse du gaz de travail, le gaz d’emprisonnement ne doit pas pouvoir être aisément ionisé. Ainsi, on utilise des éléments qui nécessitent une quantité importante d’énergie pour être ionisés. Le gaz de travail doit de plus lui aussi être peu susceptible de réagir chimiquement avec les constituants du tube, ou encore être bon marché. Finalement, les gaz nobles d’une manière générale les éléments les plus adaptés. Ceci est dû au fait qu’ils ont leur couche supérieure d’électrons entièrement remplie. Cette caractéristique fait de ces gaz de très bons « isolants ». La section « Atome » du site explique ce phénomène physique plus en détail. L’argon, le néon, le xénon et le krypton sont les plus utilisés. Le gaz d’emprisonnement joue un double rôle au sein du tube à décharge.
D’une part, le gaz d’emprisonnement facilite l’amorçage de la lampe. Contrairement au mercure et au sodium, ces éléments sont à l’état gazeux à température ambiante. Bien qu’il forme un plasma très isolant, il facilite ainsi le passage de courant électrique dans le tube à décharge, notamment au démarrage, quand les éléments principaux ne sont pas vaporisés. Ce courant électrique permet d’échauffer le tube à décharge, et ainsi vaporiser les éléments principaux (mercure, sodium, etc…). On peut d’ailleurs constater que lorsqu’une lampe à décharge démarre, par exemple lorsque les luminaires d’éclairage public s’allument dans la rue, la couleur de la lampe varie pendant les premières secondes voire les premières minutes. Au démarrage, ce sont les atomes de gaz neutre qui sont directement responsables de l’émission de lumière. Au fil des secondes, les éléments principaux se vaporisent et ce sont eux qui prennent peu à peu le relais.
Démarrage d'une lampe à vapeur de sodium sous haute pression

Une lampe à vapeur de sodium sous haute pression contient généralement un amalgame de sodium (80%) et de mercure (20%) en tant que gaz de travail, et du xénon en tant que gaz d'emprisonnement. Au démarrage, le sodium n'étant pas vaporisé (état solide), quelques électrons entre en interaction avec les atomes de xénon, donnant une faible lueur de couleur bleue. Peu à peu, le sodium se vaporise. Le rayonnement issu des intéractions entre les électrons et les atomes de sodium prend le pas sur celui issu du xénon.
D’autre part, le gaz d’emprisonnement contribue au rendement lumineux de la lampe. De la même manière qu’il facilite le passage du courant électrique au démarrage, il facilite le passage de celui-ci dans le gaz principal en régime établi. Les électrons peuvent être vus grossièrement comme des particules qui effectuent des « sauts » d’atomes en atomes, ces derniers pouvant être vus comme des « points de passage » obligés pour les électrons (à la manière d’un gué qui permettrait à quelqu’un de traverser un cours d’eau). La présence du gaz d’emprisonnement engendre de nombreuses interactions entre les atomes qui le constituent et les électrons (« collisions élastiques », sortes de « sauts » effectués par les électrons d’atomes en atomes). Ceci provoque indirectement une augmentation des interactions entre ces mêmes électrons et les ions de l’élément principal. Ces dernières sont des « collisions inélastiques », car l’électron est absorbé par l’ion. L’énergie qu’il contient est convertie sous forme de rayonnement réémis vers l’extérieur ou bien sous forme de chaleur. Ce sont ces rayonnements qui sont à l’origine de la lumière émise.
Il peut sembler paradoxal au premier abord d’utiliser un gaz neutre ayant des propriétés isolantes pour faciliter l’amorçage et augmenter le flux lumineux d’une lampe. Les collisions inélastiques dans un tube à décharge doivent en fait être dosées. Si elles contribuent à l'émission de lumière, elles augmentent aussi la température. Or, celle-ci va de pair avec la pression, qui doit rester à un niveau optimal. Les collisions inélastiques doivent se produire en nombre suffisant pour produire une quantité de lumière souhaitée, mais doivent être régulées afin de limiter la hausse température à l’intérieur de la lampe.
La solution passe par l'introduction du gaz d'emprisonnement sous haute pression, bien plus élevée que celle du gaz de travail. Les probabilités de rencontre entre un électron avec un atome du gaz d’emprisonnement et avec un atome du gaz de travail sont à peu près égales, à pressions respectives égales. Si on augmente la pression du gaz d'emprisonnement, on augmente ainsi le nombre de collisions élastiques, lesquelles augmentent indirectement le nombre de collisions inélastiques à une valeur souhaitée. Par exemple, si dans une lampe LPS la pression du néon (gaz d’emprisonnement) est de 1,5 atm et celle du sodium (gaz de travail) de 0,004 atm, les chocs entre électrons et atomes de néon sont ainsi 375 fois plus probables que ceux avec les atomes de sodium. Cela donne un nombre de collisions élastiques avec les atomes de néon très important, qui par ricochet augmente le nombre de collisions inélastiques avec les atomes de sodium, augmentant ainsi la quantité de lumière émise. Le gaz d'emprisonnement permet en plus d'assurer une bonne conductivité thermique à l’intérieur du tube, afin que la distribution thermique reste homogène (ce qui n’est pas le cas au démarrage où les parois du tube sont toujours plus froides).
Les collisions élastiques et inélastiques

Dans un tube à décharge se produisent des collisions élastiques et inélastiques. Une collision fait suite à une « rencontre » entre un électron libre et un ion ou un atome (par exemple de sodium ou de néon). Dans le cas d'une collision inélastique, l’électron, qui transporte initialement de l’énergie, cède celle-ci qui est captée par l’ion. Cette énergie peut être captée de deux manières :
Elle peut être rayonnée vers l’extérieur. Se produit un rayonnement électromagnétique, qui peut être visible. On parle dans ce cas de « lumière ».
Elle peut être absorbée par l’ion. On parle alors de transfert d’énergie cinétique, qui peut être vue comme une quantité de mouvement. Cette énergie augmente la quantité de mouvement (vibrations) de l’ion. À grande échelle, cela se manifeste par une hausse de la température.
Dans le cas d'une collision élastique, l’électron intègre l’atome mais est immédiatement réémis vers l’extérieur. Il ne se produit pas de transfert d’énergie cinétique ou par rayonnement.
Dans le cas d'une lampe LPS, les collisions inélastiques se produisent principalement avec des atomes de sodium (élément principal). Les collisions élastqiues se produisent principalement avec des atomes de néon (élément neutre). La présence du néon engendre une faible lumière rouge dans la lampe LPS au démarrage. Cette lumière est provoquée par la faible quantité de collisions inélastiques avec le néon. Par la suite, le sodium se vaporise et la plupart des collisions inélastiques se produisent avec le sodium, rendant une lumière de couleur majoritairement jaune-orangée. Une fois la lampe en régime établi, les collisions élastiques avec les atomes de néon contribuent à une meilleure circulation des électrons. Cette circulation augmente ainsi le nombre de collisions inélastiques avec le sodium.
Dans le cas d'une lampe LPS, les collisions inélastiques se produisent principalement avec des atomes de sodium (élément principal). Les collisions élastqiues se produisent principalement avec des atomes de néon (élément neutre). La présence du néon engendre une faible lumière rouge dans la lampe LPS au démarrage. Cette lumière est provoquée par la faible quantité de collisions inélastiques avec le néon. Par la suite, le sodium se vaporise et la plupart des collisions inélastiques se produisent avec le sodium, rendant une lumière de couleur majoritairement jaune-orangée. Une fois la lampe en régime établi, les collisions élastiques avec les atomes de néon contribuent à une meilleure circulation des électrons. Cette circulation augmente ainsi le nombre de collisions inélastiques avec le sodium.